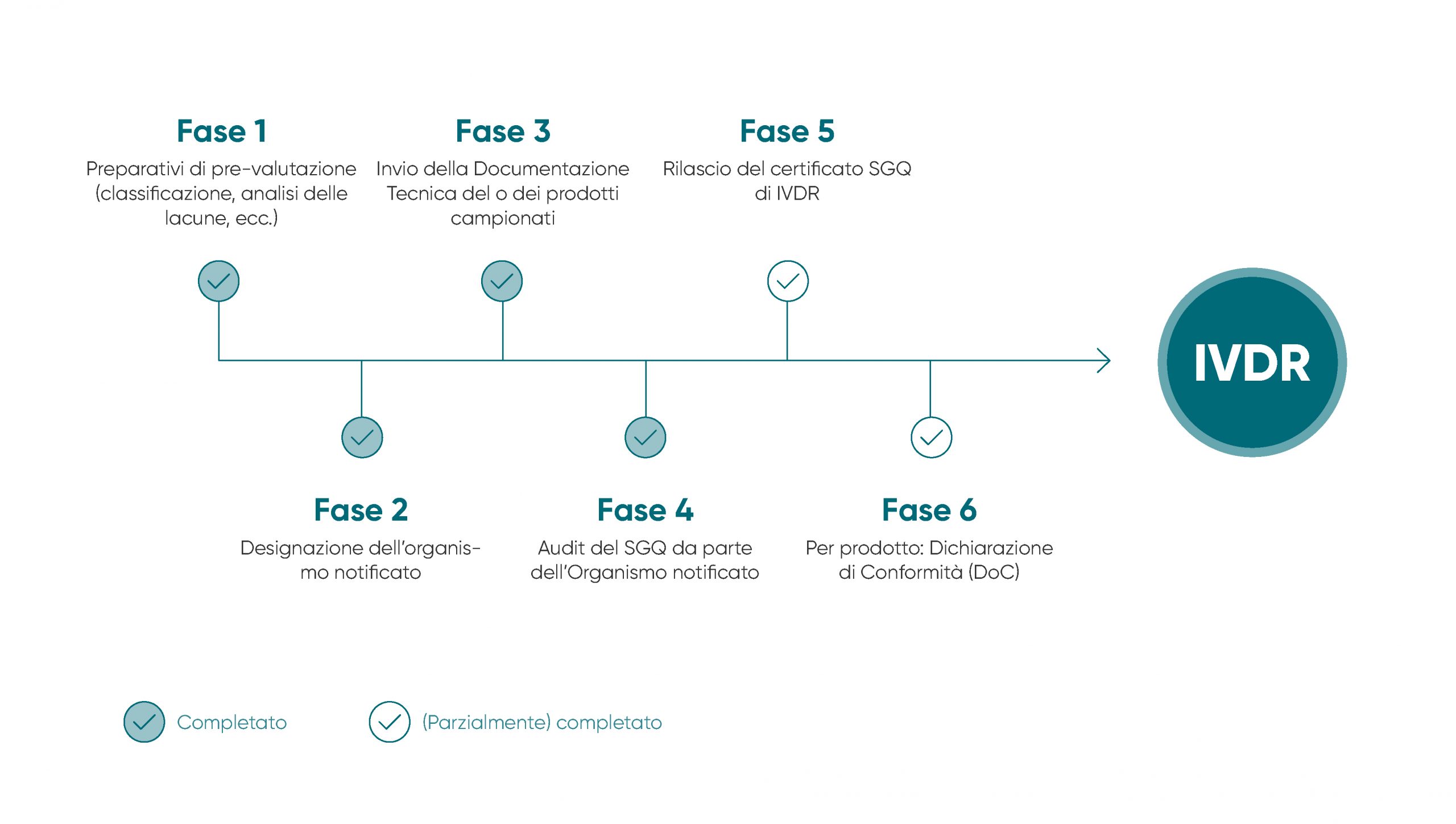
L’Ue ha creato un nuovo quadro giuridico per la qualità e la sicurezza dei dispositivi medici in vitro, ovvero l’IVDR (regolamento relativo ai dispositivi medico-diagnostici in vitro), che fissa standard più elevati, giuridicamente vincolanti per tutti gli Stati membri dell’Ue a partire da maggio 2022. Innanzi tutto, questa ordinanza migliora la sicurezza clinica dei dispositivi medico-diagnostici in vitro e definisce una base giuridica uniforme per tutti i fabbricanti.
Gli elementi chiave del nuovo regolamento sono requisiti più severi per documentazione, evidenze cliniche e valutazione della conformità, nonché trasparenza e tracciabilità dopo il lancio dei prodotti sul mercato. Con questa certificazione, i fabbricanti dimostrano di soddisfare i massimi standard di qualità e sicurezza e di disporre di un efficace sistema di gestione del rischio.
Essendo da sempre fortemente impegnata per la qualità, R-Biopharm dichiara di garantire la piena osservanza delle disposizioni dell’IVDR e impiega notevoli risorse per monitorare la piena attuazione di detto regolamento. Il nostro sistema completo di gestione della qualità ci consente di assicurare il rispetto degli standard e dei requisiti normativi, nonché l’applicazione di standard di qualità adeguatamente elevati, dallo sviluppo dei prodotti al loro utilizzo. In questo modo garantiamo un costante miglioramento della qualità al fine di fornire prodotti affidabili e di alta qualità sul lungo periodo per la salute di consumatori e pazienti.
R-Biopharm continuerà a fare fede a questo suo impegno, determinata ad affrontare le sfide future, come sancito dai valori fondamentali della nostra azienda. Naturalmente, verranno prorogati i periodi di transizione: le innovazioni dei prodotti devono essere conformi ai nuovi regolamenti dal 26 maggio 2022, mentre per i prodotti esistenti di diverse classi, tale requisito sarà richiesto soltanto a partire da fine maggio 2025 (per i prodotti in classe D), 2026 (classe C) e 2027 (classi A-sterile e B). Nonostante ciò, l’attuazione dei requisiti dell’IVDR continua ad essere una priorità assoluta in R-Biopharm.